Lelettroforesi
su gel
Le
grosse molecole organiche
hanno spesso cariche elettriche positive o negative in eccesso
localizzate sui singoli gruppi di atomi. Poiché le cariche
elettriche si sommano algebricamente, si può calcolare
la carica netta totale di ogni molecola.
 La
tecnica dellelettroforesi si basa sul fatto che, se si applica
un campo elettrico a una soluzione acquosa, le molecole
con carica totale positiva migrano verso il polo negativo, e
viceversa.
La
tecnica dellelettroforesi si basa sul fatto che, se si applica
un campo elettrico a una soluzione acquosa, le molecole
con carica totale positiva migrano verso il polo negativo, e
viceversa.
Si
deve avere la precauzione di usare una soluzione
tamponata per evitare che il campo elettrico generi
variazione di pH, modificando
la carica totale.
Questa
tecnica, nota come elettroforesi, fu originariamente
utilizzata per separare miscele di proteine,
allo scopo di caratterizzare le singole catene polipeptidiche
che le costituivano.
In soluzione
però esiste anche il fenomeno casuale della diffusione;
perciò lelettroforesi moderna è basata sullutilizzo
di un supporto solido inerte, sufficientemente poroso
da permettere il passaggio delle molecole, ma capace di evitare
che esse si disperdano in altre direzioni.
 Il
supporto è un polimero che genera una struttura a reticolo,
un "setaccio molecolare" attraverso le cui maglie
le molecole più piccole passano velocemente, mentre quelle
più grandi ritardano. La velocità di migrazione
di una molecola dipenderà quindi dalla sua forma e dimensione.
Il
supporto è un polimero che genera una struttura a reticolo,
un "setaccio molecolare" attraverso le cui maglie
le molecole più piccole passano velocemente, mentre quelle
più grandi ritardano. La velocità di migrazione
di una molecola dipenderà quindi dalla sua forma e dimensione.
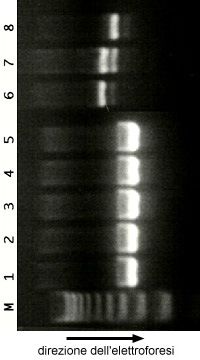
Dopo aver
applicato la tensione elettrica per un certo tempo, le diverse
molecole si troveranno quindi più o meno lontane dal
punto di partenza. Se esse non hanno un colore proprio si
dovrà applicare al supporto un colorante specifico,
per poterle individuare.
Lelettroforesi
è usata principalmente per separare miscele di proteine
e di acidi nucleici. La
comparsa di
una
traccia in una posizione inusuale, per esempio, indica che la
cellula possiede una molecola con carica o dimensione diverse
da quelle conosciute. Si può allora estrarre dal supporto
la molecola per sottoporla ad analisi chimica.
Separazione
di proteine (SDS-PAGE)
Separazione
di frammenti di DNA